前言
肾脏疾病是全球性健康问题,影响着众多人群。近年来,基于人类多能干细胞(hPSC)的肾脏类器官技术为肾脏研究带来了新的希望,但仍存在空间模式化不足、成熟度低等问题,限制了其在疾病建模和再生医学中的应用。
肾脏由超过30种不同类型的细胞组成,这些细胞在肾脏的连续管状网络中分化并执行多种生理功能。具体而言,生理条件下,肾脏的形成依赖于几种肾祖细胞之间的相互作用,其中SIX2+肾祖细胞(NPCs)和WNT11+输尿管祖细胞(UPCs)的相互作用是肾脏发育的基础。NPCs生成肾单位,而UPCs分化形成收集管(CD)网络。尽管已有研究尝试通过混合不同类型的肾祖细胞来生成类器官,但这些结构仍然缺乏成熟的肾脏功能。因此,开发具有复杂空间模式化和成熟功能的肾脏类器官模型是当前研究的重点。
2025年9月17日,南加州大学李中伟及合作团队在期刊Cell Stem Cell发表论文“Spatially patterned kidney assembloids recapitulate progenitor self-assembly and enable high-fidelity in vivo disease modeling”,成功开发出一种空间模式化的肾脏组装体(KPAs),能够在体外乃至体内重现肾脏前体细胞的自组织过程,形成与天然肾脏高度相似的结构和功能。移植体内后,KPAs可与小鼠的血液循环系统无缝对接并继续生长、发育并形成具有功能的肾脏结构,表现出良好的血管化和尿液生成能力。这不仅解决了类器官长期停留在“半成熟状态”的难题,也首次为复杂肾病的高保真建模提供了切实可行的平台。

01 从类器官到“组装体”
现有的肾脏类器官模型大多依赖单一前体细胞群体,比如利用SIX2阳性的肾单位前体细胞(NPCs)生成肾单位,或通过尿管芽前体细胞(UPCs)发育出集合管网络。虽然这些模型揭示了肾脏发育的局部过程,但由于缺乏不同前体细胞之间的相互作用,它们始终无法形成真正成熟的空间格局。李中伟团队抓住了一个关键:在胚胎发育中,肾脏的复杂结构源自不同前体细胞群体的互作——NPCs生成肾单位,UPCs形成集合管,间质祖细胞(IPCs)和血管祖细胞(VPC)则提供支持。研究者推测,只有将这些多种前体细胞以接近天然的方式汇聚,才能触发真正的“自组装”过程。
在此基础上,团队提出了“肾脏组装体”的概念。不同于传统的类器官单一分化,组装体通过将人类多能干细胞衍生的iNPCs与iUPCs在优化的培养体系中共培养,诱导它们自发组织成具有空间分区的肾脏微型结构。这种策略相当于在培养皿中重现了胚胎肾脏发育的“对话逻辑”,让细胞自己找到属于它们的“位置”。
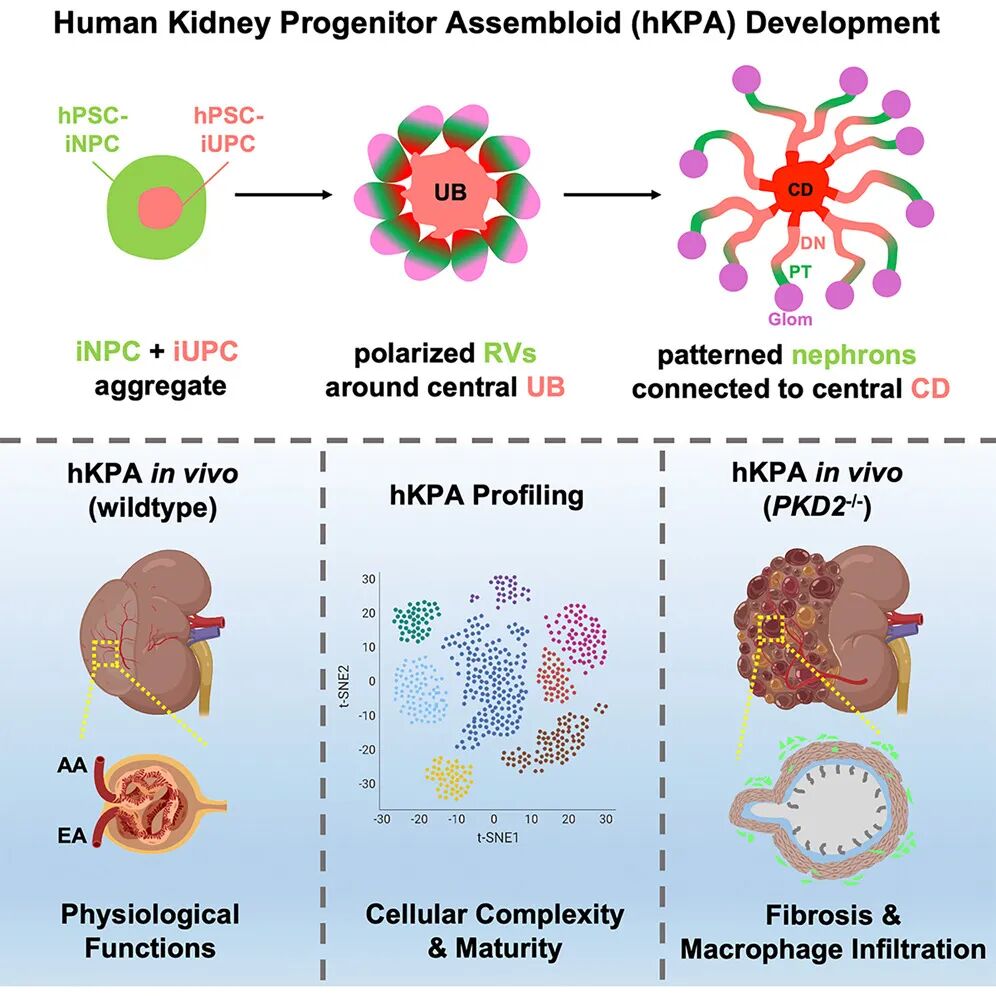
02 实验设计:从小鼠到人类
研究首先在小鼠体系中进行验证。通过改良的“v2培养基”,小鼠NPCs与UPCs能够在三周左右的时间里自发形成包含约150个肾单位的三维结构,即小鼠KPA(mKPA)。所有肾单位不仅展现出近曲小管、亨利袢、远曲小管等分段特征,还能与中央集合管网络相连,形成类似天然肾脏的连续管道。尤其值得注意的是,类器官中展现出了典型的维生素D代谢、促红细胞生成素分泌等内分泌功能,这些都是此前人类肾脏类器官无法实现的生理特征。
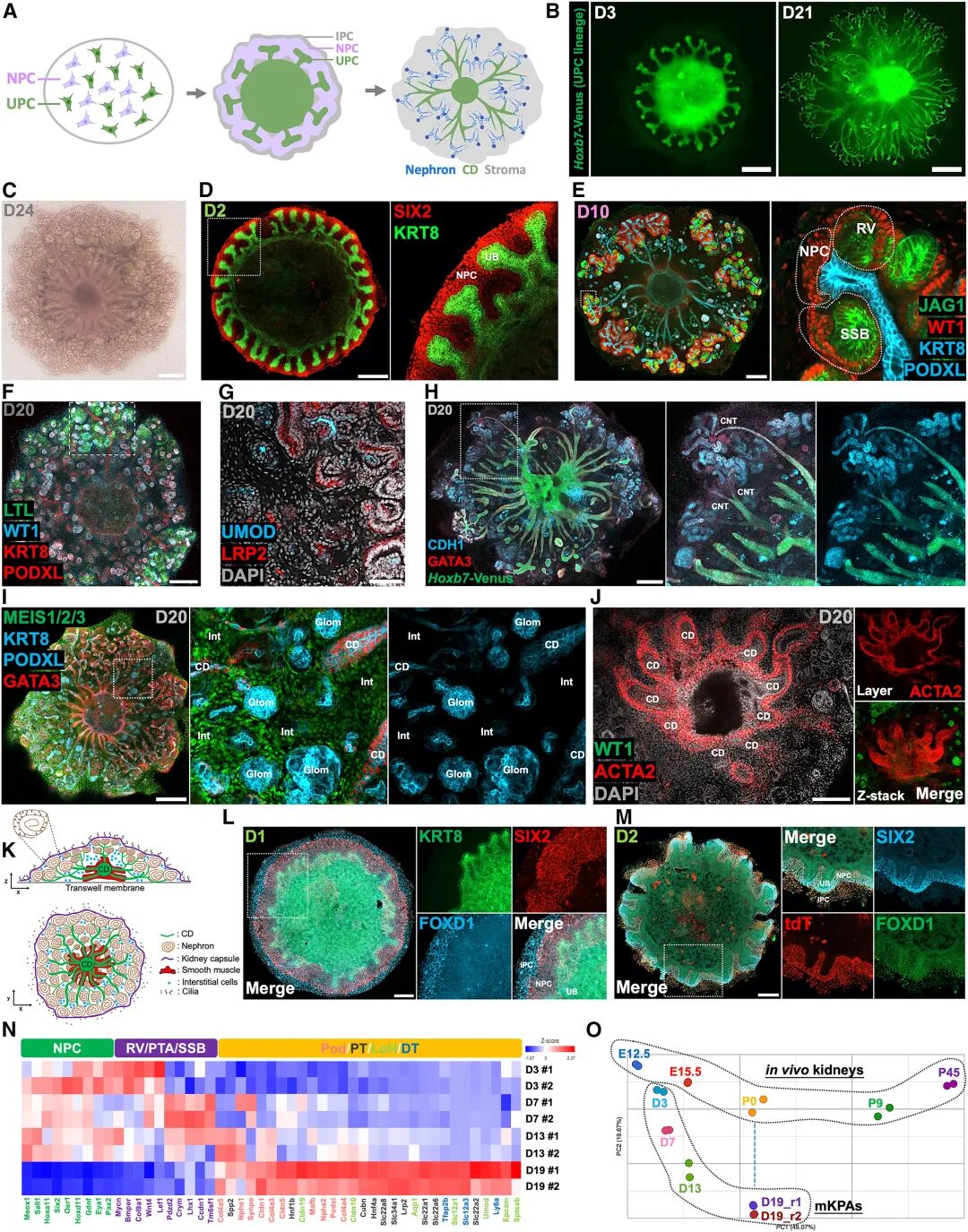
图 :由可扩展的 NPC 和 UPC 组装成 小鼠KPA(mKPA)
在人类体系中,研究团队进一步建立了“v3培养基”(在v2基础上缩短了FGF9的处理时间,并添加了激素氢化可的松21-半琥珀酸酯(HCHS)和A83-01),并在其中成功组装了空间模式化的人源肾脏组装体(hKPAs)。这些hKPAs同样形成了极化的肾泡,逐步分化为分节的肾单位,并与中央集合管对接。此外,尤其值得注意的是,该培养方案具有高度可重复性,在多个iPSC系中均能建立。
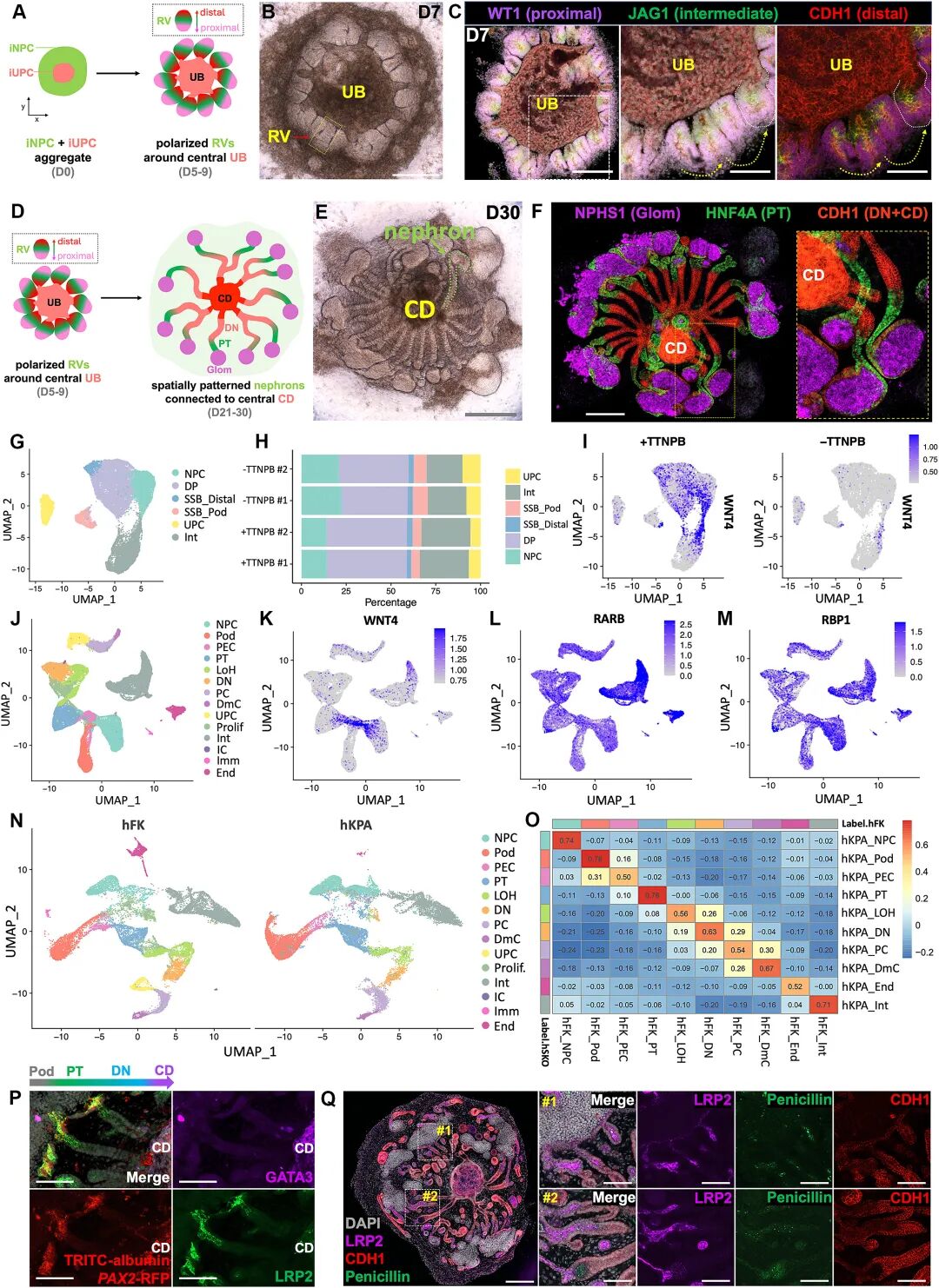
图:iNPC 和 iUPC 的空间模式化 hKPA 组装
03 核心突破:空间格局与功能成熟
通过单细胞组学和多组学联合分析,研究团队证实,这些组装体在转录谱和染色质开放状态上都高度接近新生鼠肾脏和17周的人类胎儿肾脏。
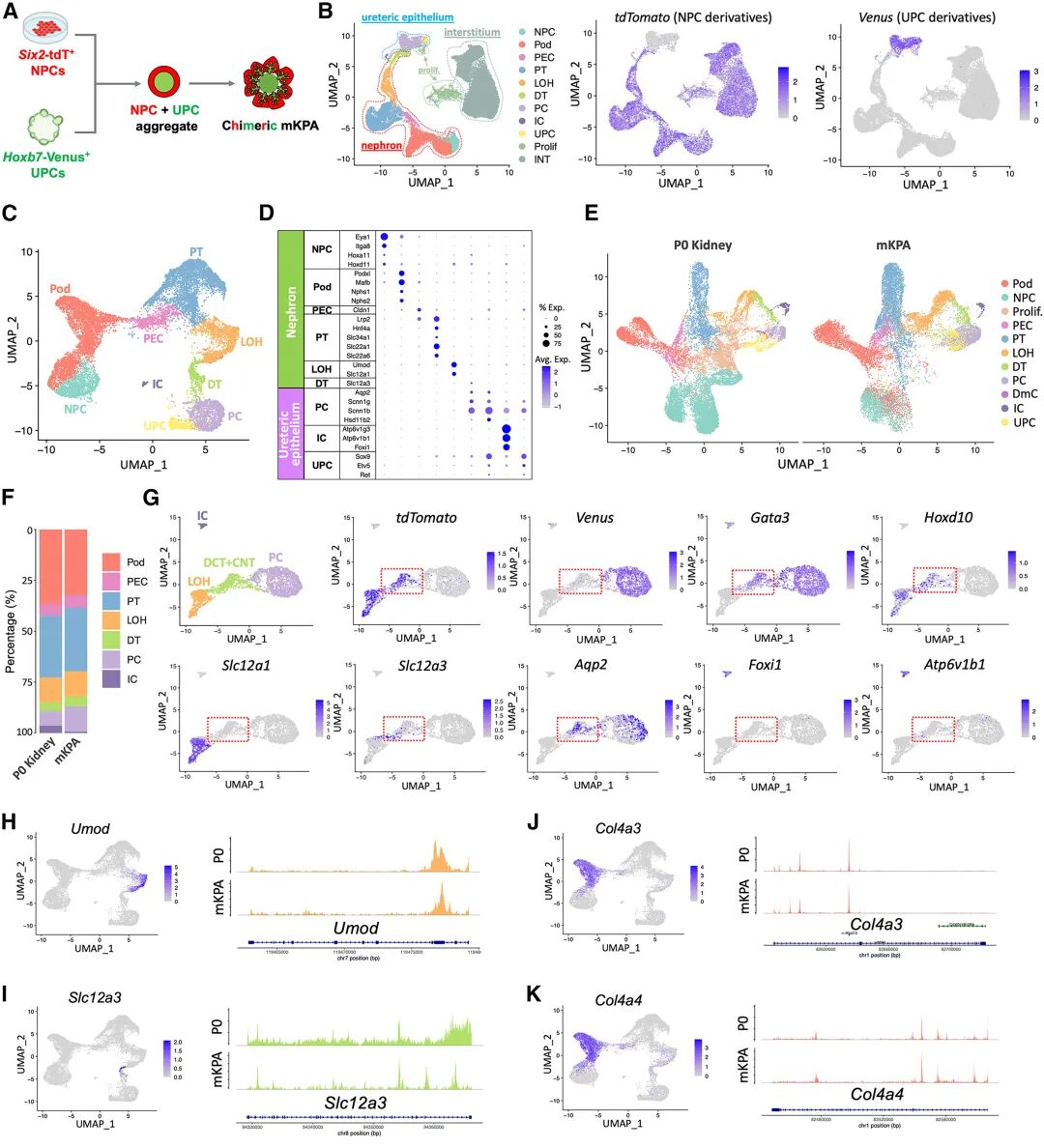
图:mKPAs 的单细胞多组学分析
相比传统类器官,KPAs不仅包含集合管细胞类型,还在代谢通路上表现出更强的氧化磷酸化能力,提示能量代谢向成熟肾小管靠拢。移植到小鼠体内后,hKPAs表现出进一步的成熟,形成了人源性血管、间质和肾小球结构,展现了真正的灌注和滤过功能。
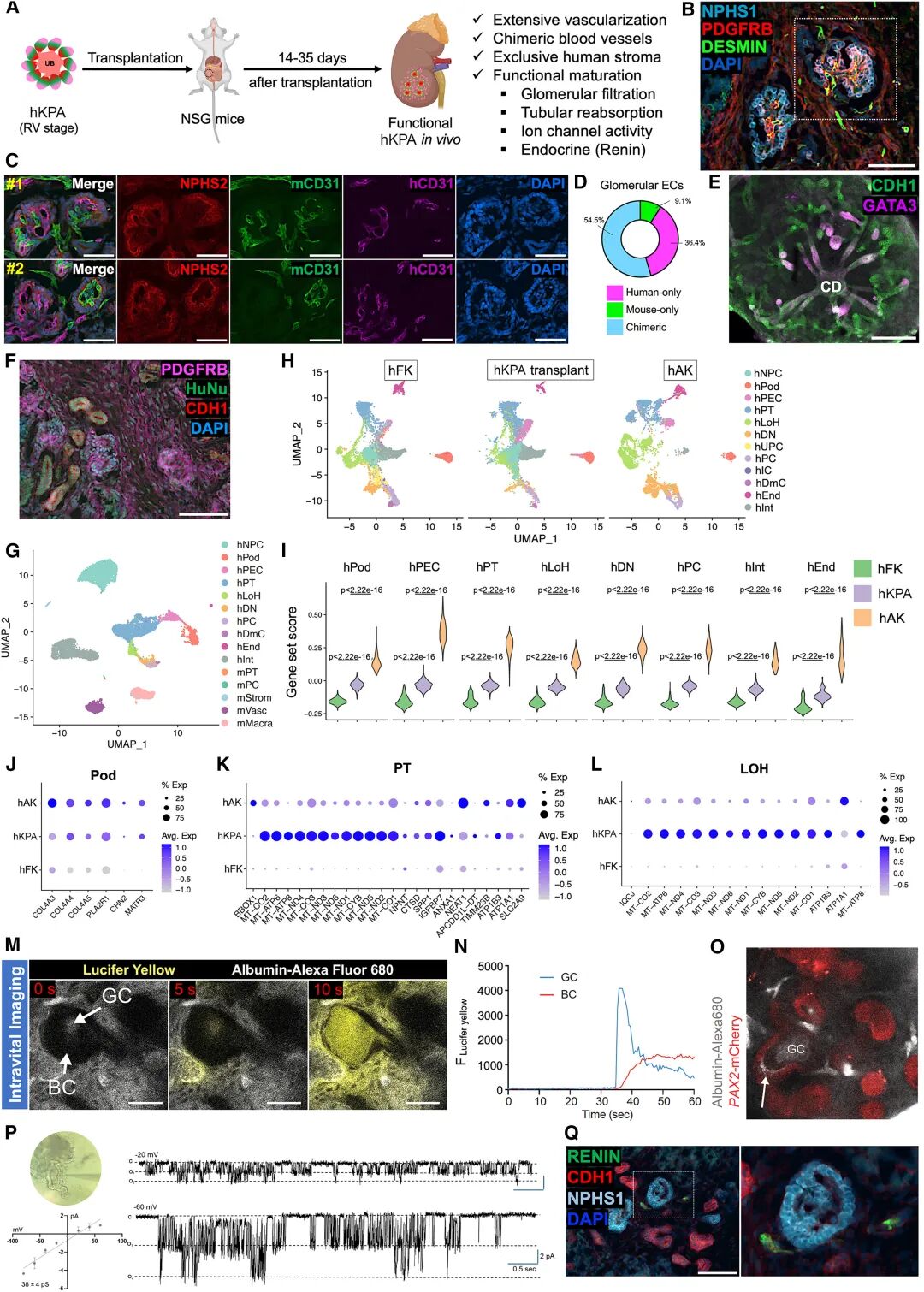
图:体内移植后功能性hKPA的生成
这种成熟度的提升带来了关键意义:它不仅仅是“结构像”,更是“功能像”。过去的肾脏类器官常被诟病停留在胚胎早期,无法模拟成人期疾病。而KPAs在体内环境中展现的功能,使其成为一个能够跨越“发育—疾病—再生”全链条的研究平台。
04 疾病建模:ADPKD的高保真复现
为了验证平台的应用潜力,研究团队选择了最常见的遗传性肾病——常染色体显性多囊肾病(ADPKD)。结果显示,基因编辑后(PKD2-/- hKPAs)的组装体不仅在两个月内生长至接近宿主肾脏的体积,还出现了典型的囊性结构,囊液中肌酐和尿素浓度显著升高,与患者表现高度一致。更重要的是,PKD2-/- hKPAs中观察到囊上皮极性的丧失、周围基质细胞的纤维化以及巨噬细胞浸润,这些复杂的细胞间互作是现有体外类器官模型完全无法再现的。
单细胞测序进一步揭示了PKD2-/- hKPAs中关键致病通路的激活,包括cAMP、PI3K/AKT、mTOR以及Wnt信号,同时氧化磷酸化水平显著下降。这些分子特征与患者样本高度吻合,为阐释疾病机制和寻找潜在靶点提供了窗口。
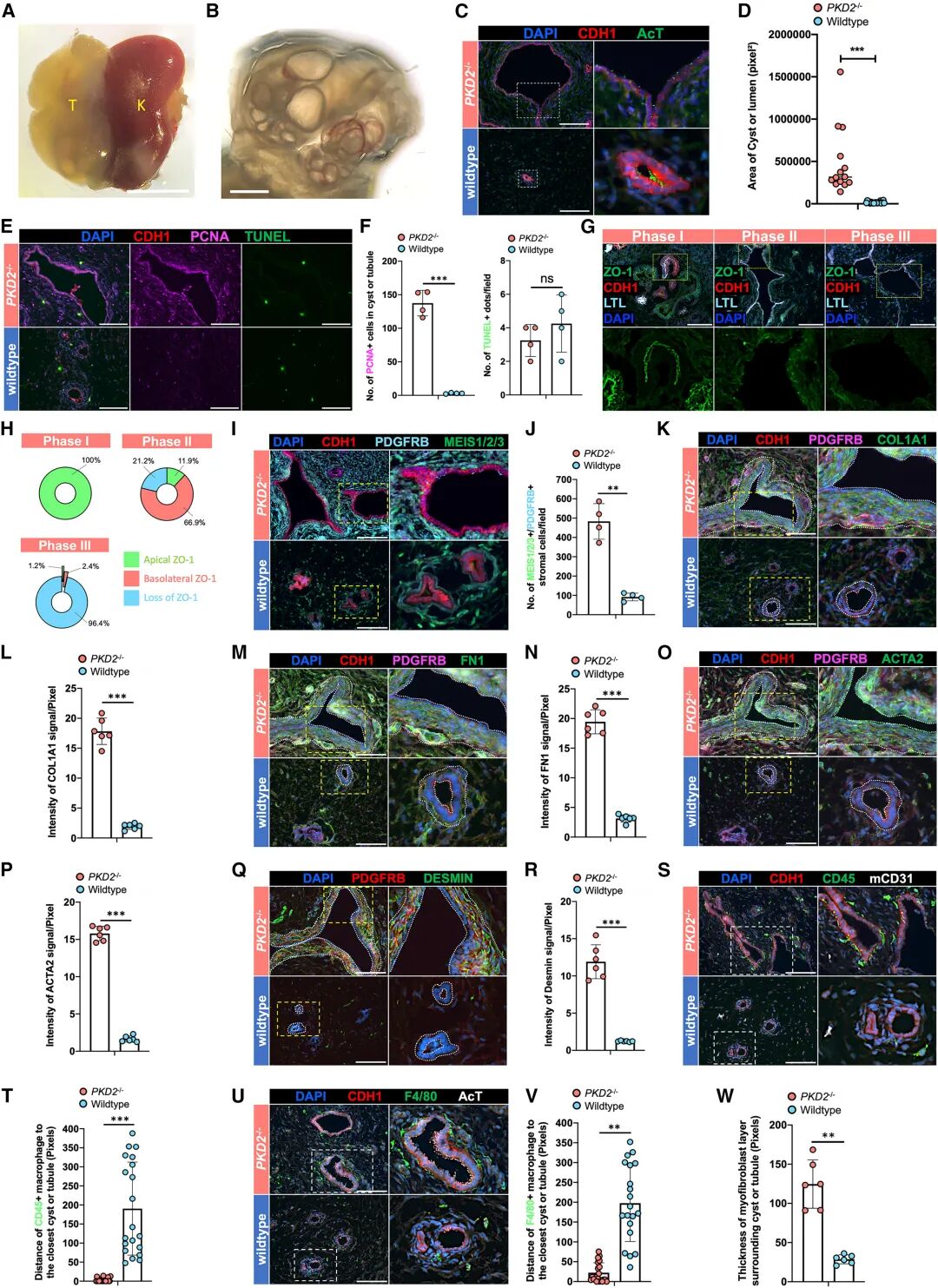
图:人类 ADPKD 与PKD2−/− hKPA的高保真体内模型
05 总结
本研究重要性在于,它为肾脏疾病研究打开了全新的可能性。空间模式化的组装体不仅能真实反映复杂疾病的进展过程,也能成为药物筛选和疗效预测的高保真平台。在再生医学领域,这种策略更为人造肾脏的构建提供了坚实基础。通过不断优化培养体系与前体细胞的互作模式,未来或许能够在实验室中生成具备完整功能的肾脏,用于替代衰竭的器官。
近岸蛋白相关产品
近岸蛋白提供多种类器官体外培养全方案,包括基质胶、培养基、相关细胞因子等:
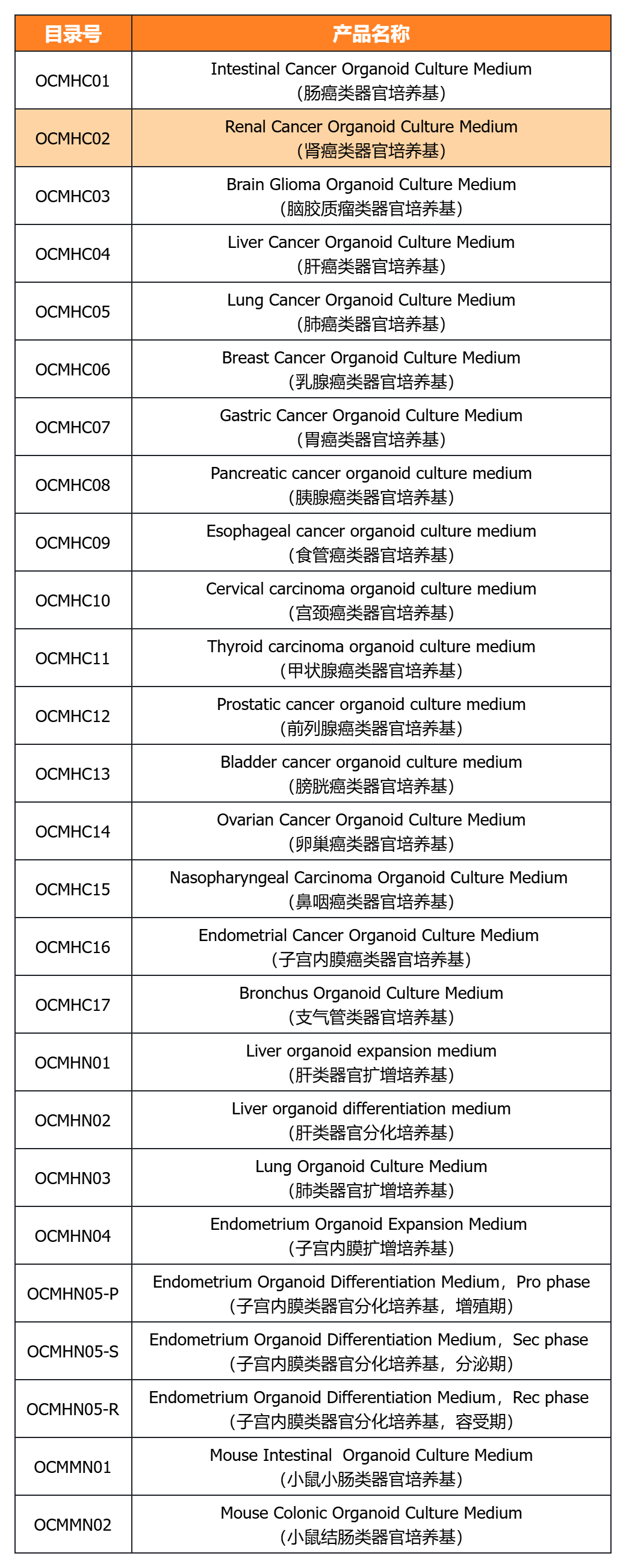
经类器官培养验证的完全培养基
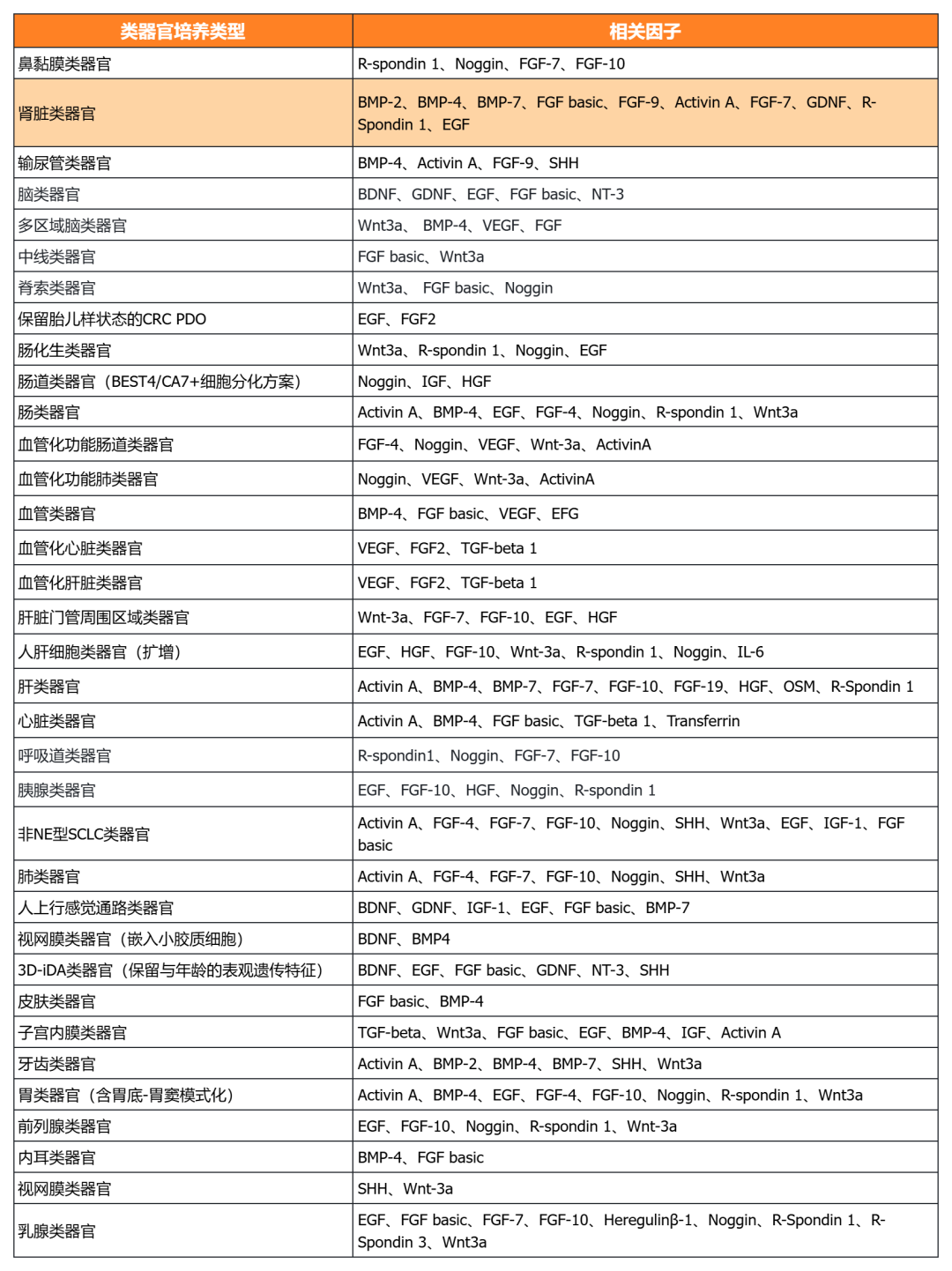
经类器官培养验证的细胞因子
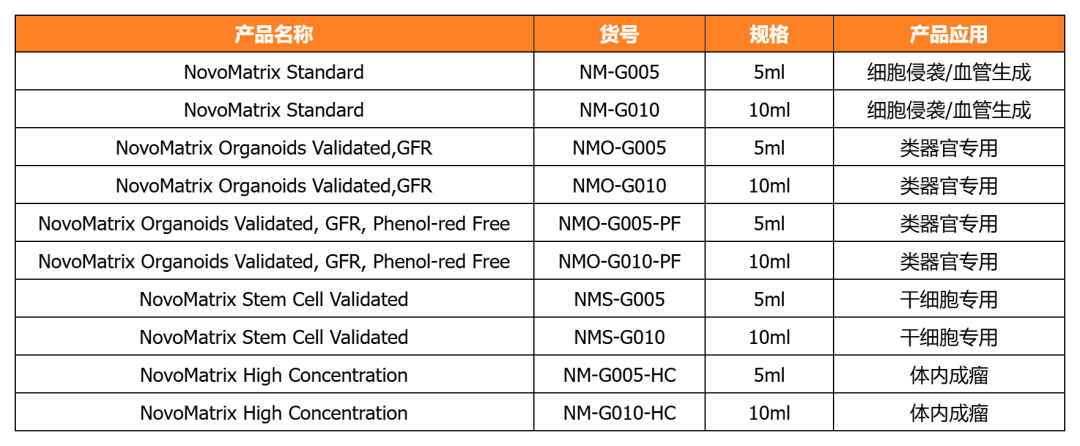
NovoMatrix 基质胶
参考资料
Huang B, Medina P, He J, et al. Spatially patterned kidney assembloids recapitulate progenitor self-assembly and enable high-fidelity in vivo disease modeling. Cell Stem Cell. Published online September 17, 2025. doi:10.1016/j.stem.2025.08.013
